Баланс и наличие каждого элемента строго выверен.. и при значительном дисбалансе.. хорошего результата не получить.. увы...
Гидропоника - точная технология.
Строго контролируемая, предсказуемая.
Вариант - кинул две ложки на банку воды... - не пройдет
Основа питания растения - всего 5 элементов
Кальций- азот-фосфор-калий-магний - это макро элементы.
Возможно использовать не отдельные соли... а так называемые "комплексные удобрения"
сразу предупрежу, из комплексных не всегда возможно приготовить "правильный раствор"
всегда будет чего-то не хватать а чего-то будет избыток.
На комплексных удобрениях стоит маркировка...
в формате N-P-K-Mg
именно в такой последовательности их содержание пишут на пачках с удобрениями
вот например 30.10.10

означает что азота 30% Фосфора 10% Калия 10% а Магния в нем нет..
если написано (к примеру!) 30-0-25-5
то соответственно азот 30%, фосфор 0%, калий 30%, магний 5%
Есть неприятность.. производитель не всегда указывает это содержание ЧИСТОГО элемента или в пересчете на ОКСИД. но можно эту информацию добыть.. или на сайте производителя или по телефону.. они охотно делятся.
Если указано содержание оксида - то нужно будет самостоятельно пересчитать в чистый элемент.
В рецептах растворов обычно указывается конкретно что за цифры вы видите (могут быть моль на литр, могут быть милиграммы на литр), и чего именно оксида или элемента.
мы будем использовать миллиграммы и массы чистых элементов
На простом примере покажу как рассчитать массу элемента в известной нам соли:
Предположим нам необходимо узнать сколько Калия и сколько Фосфора в Монофосфате калия
кислород, водород не учитывается в растворах..
Формуа монофосфата калия К4Р2О7
это означает что в одной молекуле нашей соли калия четыре атома, фосфора два, кислорода семь
теперь идем в табличку Менделеева и находиматомные массы наших элементов.
(массы округляем до целых для удобства.. погрешность минимальна)
К(калий) 39
Р(фосфор) 31
О(кислород) 16
Значит атомный вес всего соединения К4Р2О7 будет равен 39*4+31*2+16*7=330
это 100% вещества
теперь вычисляем сколько процентов из него Калий и сколько Фосфор
Всего
калия 39*4=156 (из 330)
фосфора 31*2=62 (из 330)
простой расчет процентовочки
100%/330*156=47,27%
Значит в одном грамме порошка 472,7 мг чистого калия.
100%/330*62=18,79%
В 1 грамме порошка 187,9 мг чистого фосфора.
И да, это НЕ ХИМИЯ
таким образом можно пересчитать любое вещество..
случается иметь дело не с просто солями.. а кристаллгидратами.
например сульфат магния чаще всего кристаллгидрат..
он отличается от просто сульфата тем, что в нем очень много атомов водорода и кислорода - сгруппированных в молекулы воды.. нет, он не жидкий... просто химики все H2 и О которые могли бы составить молекулу воды.. сгруппировали и записывают так MgSO4•7H2O как видно в нем 7 молекул воды.. так и говорят семиводный сульфат магния
и магния там значительно меньше чем в просто сульфате.. при расчете это нужно учитывать:
то есть у нас:
Mg (магний) один атом
S (Сера) один атом
О (кислород) 4+7
H(водород) 2*7
можно было бы записать эту формулу так MgSO11H14
естественно в расчете массы молекулы нужно учитывать вес ВСЕХ элементов
а потом уже вычислять процент Магния и Серы (это домашнее задание вам..
в принципе, все это давно посчитано и этими расчетами-пересчетами заниматься придется редко..
но случаются казусы.. и люди теряются.. паникуют
появляются вопросы .. типа у меня указано в оксиде.. как посчитать чистый элемент?
просто.. точно так же..
если указан оксид фосфора P2O5
так и считаем..
массу двух фосфоров 31*2=62
и массу пяти кислородов..... 16*5=80
складываем 62+80=142
делим 100% на то что получилось 100%/142=0.704 и умножаем на массу двух фосфоров... фосфора 0.704*62=43%
вуаля..в одном грамме оксида фосфора - 430мг чистого фосфора.
и это тоже не химия ))
сложно?
думаю нет.
С солями разобрались..
Теперь, зная сколько и какого элемента в каждом из имеющихся у нас веществ... можно составлять раствор.
Состав элементов для укропа
все в мг на 1 литр раствора
N 252,8
P 43,6
K 276,39
Ca 228
Mg 49,5
B 0,34
Fe 5,5
Mn 0,33
Zn 0,3
Cu 0,075
вот была бы халва.. сидеть считать на бумажке сколько чего нужно всыпать чтоб получилось +- столько сколько написано да
для этого существуют специальные калькуляторы.
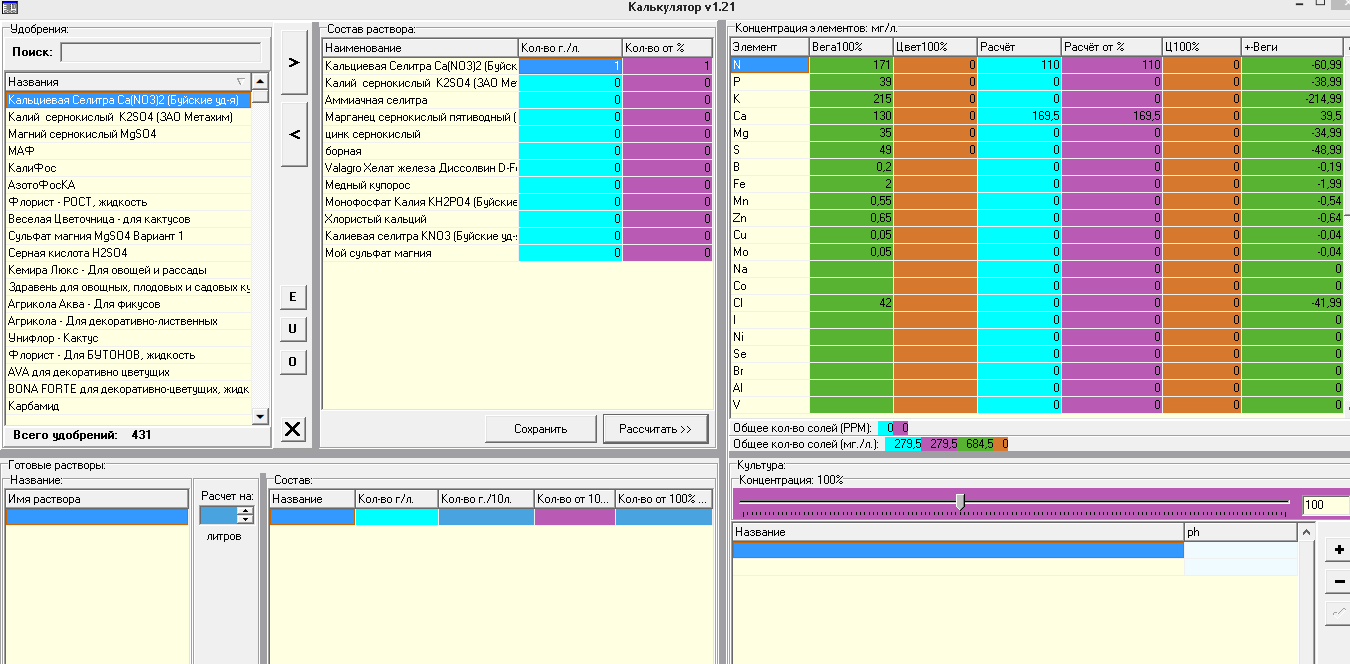
Добавляем из списка слева удобрения что у нас есть...
Вносим в средней табличке количество планируемого удобрения в граммах на литр..
жмем кнопку "рассчитать"
На картинке я "положил" в раствор 1 грамм на литр кальциевой селитры и в правой части, в столбце расчет окне наблюдаем азота 110 мг на литр, кальция 169.5 мг на литр.. мало? - добавим.. много? - убавим..
так и подгоняем чтоб все было приблизительно равно тому что нам нужно.
Калькулятор во вложении. можно скачать и изучить его работу. установка не требуется.
 NPKMg.zip 1,28МБ
20 Количество загрузок:
NPKMg.zip 1,28МБ
20 Количество загрузок:рецепты и составы можно сохранять.. изменять.. в общем это отдельная тема.. в архиве есть инструкция..
Вадик, ты усложняешь! ты просто скажи сколько вешать в граммах?
а я откуда знаю что у вас есть?
у меня например есть это:
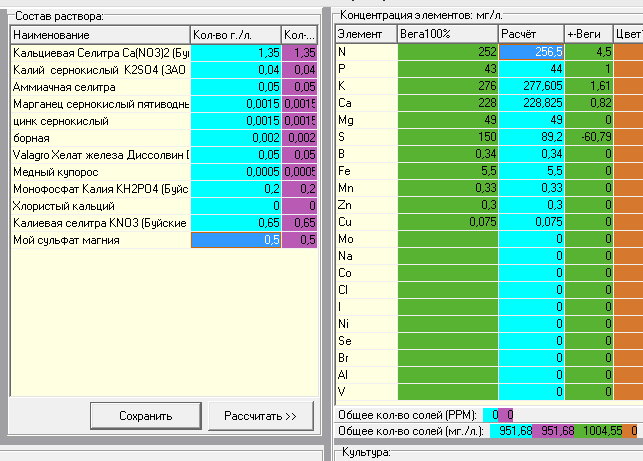
как видите, из отдельных солей легко составляется то что нужно..
итого.. на 1 литр раствора мне понадобится:
Название Кол-во г/л.
Кальциевая Селитра 1,35
Калий сернокислый 0,04
Аммиачная селитра 0,05
Монофосфат Калия 0,2
Калиевая селитра 0,65
Мой сульфат магния 0,5
Марганец сернокислый пятиводный 0,0015
Цинк сернокислый 0,0015
борная к-та 0,002
Valagro Хелат железа Диссолвин D-Fe-11 (DTPA) 0,05
Медный купорос 0,0005
Многие спрашивают а не страшно что... раствор.. химия.. яды..
Нет не страшно...
концентрация микроскопическая..
вес всех солей на 1 литр 2.8 грамма(в 1 килограмме колбасы селитры столько, что на ней можно вырастить 3 поколения укропа
как видите.. раствор в принципе можно пить.
3 грамма поваренной соли растворите в 1 литре воды.. попробуйте на вкус
вы даже не почувствуете, что вода соленая ))
Продолжение следует...
(Приготовление питательного раствора, контроль и коррекция)
Сообщение отредактировал Vad: 22 Март 2015 - 04:56




























